Molaritas adalah salah satu cara untuk menyatakan konsentrasi dari sebuah larutan. Molaritas atau konsentrasi molar menyatakan jumlah mol zat yang terlarut dalam setiap liter larutan.
Dalam kimia, satuan yang paling umum digunakan untuk molaritas adalah jumlah mol per liter (mol/L). Contohnya: suatu larutan dengan konsentrasi 1 mol/L dikatakan sebagai 1 molar, biasanya dinyatakan sebagai 1 M.
Rumus Molaritas
Untuk mempermudah menghitungnya, silahkan pelajari rumus molaritas di bawah ini!
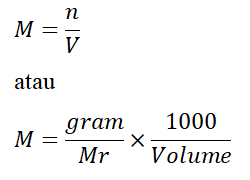
Keterangan:
- M : molaritas zat (mol/liter atau Molar)
- n : mol suatu zat (mol) atau massa/Mr
- V : volume larutan (ml)
Setelah memahaminya, yuk coba kerjakan contoh soal-soal molaritas yang disadur dari soal UN (ujian nasional), soal ujian sekolah, dan soal UTBK SBMPTN berikut ini.
Contoh Soal 1
Berapa molaritas larutan glukosa yang terkandung dalam 200 mL larutan dan memiliki kandungan 2 gram glukosa?
Pembahasan:
Diketahui:
massa glukosa = 2 gr
V.Larutan = 200 mL = 0,2 L
Mr glukosa = 180 gr/mol
Ditanya: M = ?
Jawaban:
jumlah mol glukosa = massa/Mr
jumlah mol glukosa = 2 gr /(180 gr/mol)
jumlah mol glukosa = 0,01 mol
M = jumlah mol/V
M = 0,01 mol /0,2 L
M = 0,05 mol/L
Jadi, molaritas larutan glukosa tersebut adalah 0,05 mol/L.
Contoh Soal 2
Hitung molaritas larutan asam sulfat 25% (massa) dengan massa jenis 1,178 g/mL dan Mr sebesar 98!
Pembahasan:
Diketauhi:
Misalkan massa larutan 100 gram,
massa (H2SO4) = 25% x 100 gr = 25 gram
n(H2SO4) = m / Mr
n(H2SO4) = 25 / 98
= 0,255 mol
Ditanya: Molaritas larutan asam 25% (M)?
Jawab:
Untuk menentukan Molaritas, kita harus mencari volume larutan terlebih dahulu.
V = m/ρ
V = 100/1,178
V = 84,89 mL
V = 0,08489 L
Selanjutnya, baru kita hitung Molaritasnya.
M = n / V
M = 0,255 / 0,08489
M = 3,00 mol/L
Jadi, molaritas larutan asam sulfat (H2SO4) 25% adalah 3,00 mol/L
Contoh Soal 3
Hitunglah molaritas dan molalitas NH3 dalam larutan yang mengandung 30 gram NH3 dalam 70 gram air. Kerapatan larutannya adalah 1,83 g/ml.
Pembahasan:
Diketauhi:
massa NH3 = 30 g
massa H2O = 70 g
ρ larutan NH3 = 1,83 g/mL
Mr NH3 = 17 g/mol
Jawab:
1. Molalitas NH3
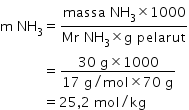
2. Molaritas NH3

Dari perhitungan di atas, didapatkan molalitas dan molaritas NH3 masing-masing sebesar 25,2 mol/kg dan 32,3 mol/L.
Contoh Soal 4
Diketahui sebuah Molaritas dari Larutan NaCl sebesar 0,4 M pada air sebanyak 40 L tentukan banyak mol NaCl yang terlarut pada Air tersebut.
Pembahasan:
Diketauhi:
Molaritas = 0,4 M
V = 40 L
Ditanyakan: Besar mol NaCl (n)?
Jawab:
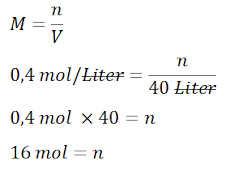
Jadi, molaritas larutan NaCl tersebut adalah 16 mol.
Contoh Soal 5
Tentukan volume air yang diperlukan untuk melarutkan 2 mol KOH (Ar K = 39, O = 16, H = 1) dalam membentuk larutan KOH 0,05 M.
Pembahasan:
Diketauhi:
M = 0,05 M
n = 2 mol
Jawab:
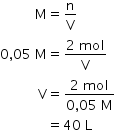
Jadi, Volume air untuk membentuk KOH 0,05 M adalah 40 liter.
Contoh Soal 6
Suatu asam sulfat pekat mengandung 96% H2SO4 (Mr = 98) dan memiliki massa jenis 1,8 kg/L. Berapakah molaritas larutan asam sulfat tersebut?
Pembahasan:
Diketauhi:
Kadar H2SO4 pekat = 96 %
Massa jenis = 1,8 kg/L
Mr H2SO4 = 98
Jawab:

Jadi molaritas larutan asam sulfat tersebut sebesar 17,6 mol/L.
Contoh Soal 7
Tentukan konsentrasi molaritas HCl yang diperoleh ketika mencampurkan 7 liter HCl 0,3 M dengan 500 ml HCl 0,2 M!
Pembahasan:
Diketauhi:
VA = 7 liter
VB = 0,5 liter
MA = 0,3 M
MB = 0,2 M
Jawab:
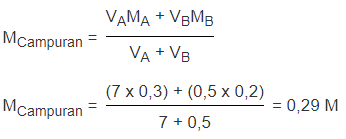
Contoh Soal 8
Tentukan molaritas larutan yang dihasilkan dari melarutkan 50 gram CaCO3 (Ar Ca = 40; Ar C = 12; Ar O = 16) dalam 500 mL air!
Diketauhi:
massa CaCO3 = 50 gram
Mr CaCO3 = 100
V = 500 mL
Jawab:


Jadi molaritas larutan tersebut adalah 1 M.
Contoh Soal 9
Hitunglah molaritas larutan Al2(SO4)3 yang dihasilkan dari pelarutan 171 gram dalam 500 mL air untuk keperluan praktikum laboratorium! (Ar Al = 27, Ar S = 32, dan Ar O = 16)
Pembahasan:
Diketauhi:
m Al2(SO4)3 = 171 gram
V = 500mL = 0,5 liter
Ar Al = 27
Ar S = 32
Ar O = 16
Ditanya: Molaritas Larutan Al2(SO4)3?
Jawab:
Cari besar Mr Al2(SO4)3 terlebih dahulu.
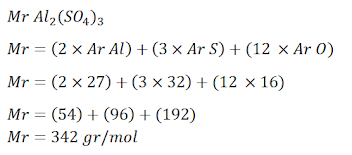
Setelah mengetauhi besar Mr Al2(SO4)3, baru cari molaritas larutannya
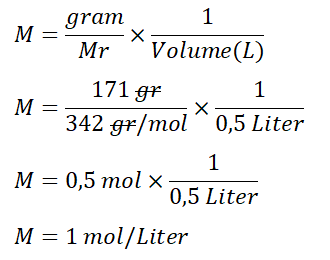
Jadi, besar molaritas larutan Al2(SO4)3 tersebut adalah 1 M atau 1 mol/Liter.

